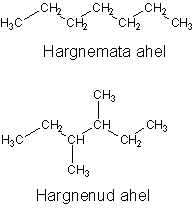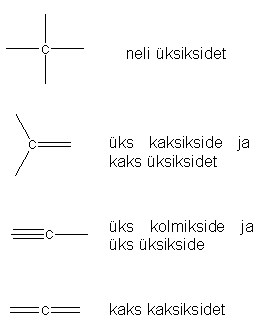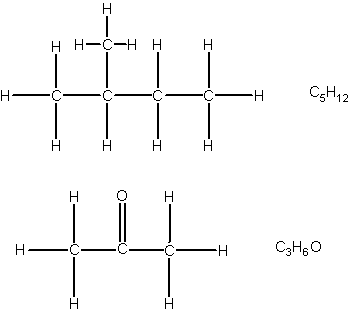Süsinikuühendite struktuur ja selle kujutamise viisid
Süsinikuühendite struktuur
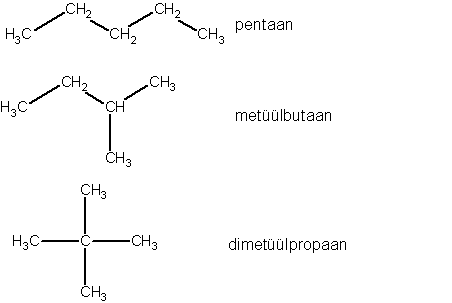
Süsinik võib moodustada väga palju erinevaid ühendeid, kuna süsinik-süsinik kovalentne side on väga püsiv ning seetõttu saavad tekkida erineva pikkuse ja kujuga süsiniku ahelad. Süsiniku ahelad võivad olla hargnemata, kui ka hargnenud (vt joonis).
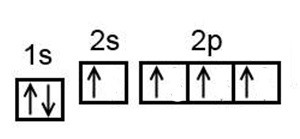
Süsiniku väliskihis on neli elektroni, mis on kõik samaväärsed – süsiniku aatom on kõige stabiilsem siis, kui üks s alakihi kihi elektron on liikunud p alakihile, nii et igale väliskihi orbitaalile jääb üks paardumata elektron.
Sulle võivad huvi pakkuda need õppematerjalid:
Ioonid
Tutvus keemiaga
Знакомство с химией
Ионы
Растворы
Lahused
Oksüdatsiooniaste
Aatomid ja molekulid
Атомы и молекулы
Kuna süsinikul on väliskihil neli paardumata elektroni, siis moodustab süsinik ühendites neli kovalentset sidet. Süsinik võib moodustada nii üksiksidemeid, kui ka kordseid sidemeid. Erinevad võimalused, kuidas süsinik saab sidemeid moodustada on toodud allpool.
Süsiniku ahelad võivad olla ka kinnised ehk tsüklilised ning sisaldada peale süsiniku veel ka teisi elemente. Peamised elemendid, millest orgaanilised ained koosnevad on C, H, O, N ja halogeenid.
Orgaaniliste ühendite kujutamise viisid
Orgaaniliste ühendite kirjutamisel ei kasutada summaarset valemit, kuna see ei anna aine struktuuri kohta infot ning üks ja sama summaarne valem võib vastata mitmele erinevale ainele. Näiteks valemile C5H12 vastab kolm erinevat struktuuri.
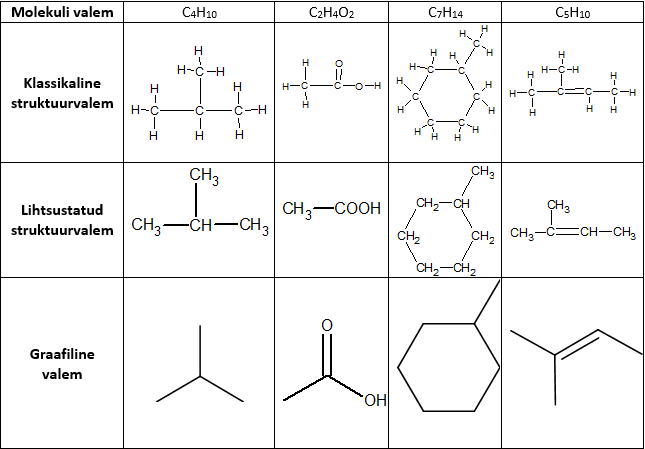
Seega kasutatakse orgaaniliste ainete kujutamiseks struktuurvalemeid – valemeid, mis näitavad ära, kuidas erinevad aatomid on molekulis omavahel seotud. Erinevaid struktuurvalemite märkimise võimalusi on mitmeid. Kõige detailsema ülevaate annab klassikaline struktuurvalem, kus kõik aatomid kirjutatakse eraldi välja ning kovalentset sidet aatomite vahel tähistatakse kriipsuga.
Kuna klassikaline struktuurvalem on väga kohmakas ning selle kirjutamine võtab palju aega, siis leiab palju rohkem kasutust lihtsustatud struktuurvalem ehk lühendatud struktuurvalem. Selles valemis vesinike eraldi välja ei kirjutata, vaid vesinikud kirjutatakse süsiniku aatomi kõrvale, näidates indeksiga ära, mitu vesiniku aatomit on süsinikuga seotud. Kõik teised elemendid kirjutatakse välja.
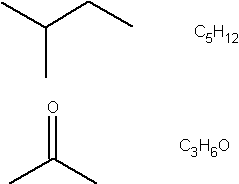
Veelgi lihtsam struktuurvalem on graafiline valem, kus süsiniku aatomeid välja ei kirjutata, vaid kujutatakse ainult sidemeid süsiniku aatomite vahel – iga murdekoht ning vaba sideme ots tähendab süsiniku aatomit. Seda, mitu vesiniku aatomit on iga süsinikuga seotud, tuleb välja sellest, et süsinik moodustab kokku neli sidet – kõik väljakirjutamata sidemed tähendavad seda, et seal on vesinik. Kõik teised aatomid (lämmastik, hapnik, halogeenid) kirjutatakse sümboliga välja ja näidatakse sidemega, millise süsiniku aatomiga ta seotud on.
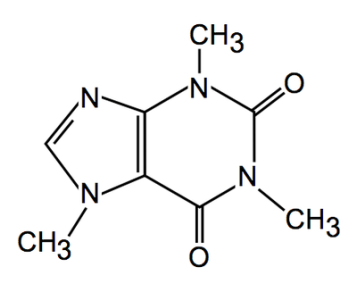
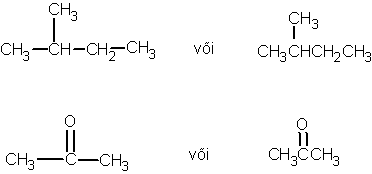
Mõningate ainete erinevad struktuurvalemid:
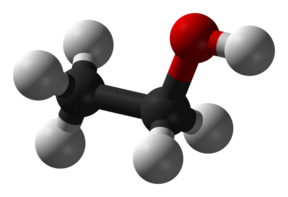
Kõik need struktuurvalemid ei kajasta seda, milline on molekuli ruumiline struktuur. Molekuli ruumilist struktuuri saab kajastada molekulimudelitega. On olemas mitmeid programme, millega saab molekuli mudeleid koostada ning nende ruumilist ehitust uurida, kuid koolides on olemas ka molekulimudelite komplektid, millega saab ise erinevaid struktuure kokku panna ning molekuli ruumilist ehitust uurida.
VIDEOD:
Struktuurvalemid ja brutovalemid (ing)
Lisainfo
- Molekulide vaatamise programm – http://chemicum.com
Märkasid viga? Anna sellest teada ja teeme TaskuTarga koos paremaks!