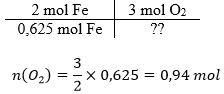Arvutused reaktsioonivõrrandite järgi
Reaktsioonivõrrandi järgi on võimalik leida seda, kui palju aineid kulub/tekib keemilise reaktsiooni käigus. Arvutused põhinevad sellel, et reaktsioonivõrrandis näitavad kordajad aine moolide suhet. Näiteks võrrand:
4Al + 3O2 = 2Al2O3
näitab seda, et 4 mooli alumiiniumi reageerimiseks kulub 3 mooli hapniku ning tekib 2 mooli alumiiniumoksiidi. Teades aine moole, on kerge arvutada aine massi (või gaasiliste ainete korral ruumala) kasutades moolarvutuse valemeid:
Sulle võivad huvi pakkuda need õppematerjalid:
Tutvus keemiaga
Aatomid ja molekulid
Oksüdatsiooniaste
Ioonid
Знакомство с химией
Ионы
Lahused
Растворы
Атомы и молекулы
Reaktsioonivõrrandil baseeruvate ülesannete lahendamisel on mõistlik järgida järgmisi etappe
- Kirjutage ja tasakaalusta reaktsioonivõrrand
- Kirjutage reaktsioonivõrrandi kohale ülesandes antud ja otsitava aine kohta toodud andmed
- Leidke nende ainete molaarmassid, mille kogus on antud või mille kogust soovitakse leida
- Leidke nende ainete moolid, mille mass (või gaasilise aine ruumala) on antud
- Reaktsioonivõrrandi kordajate suhte järgi leidke otsitud aine moolid
- Leidke küsitud aine mass (ruumala)
Näidisülesanne: Mitu liitrit hapnikku kulub 35 grammi raua roostetamiseks, kui rauast tekib raud(III)oksiid?
Lahendus:
1. Kirjutame ja tasakaalustame reaktsioonivõrrandi:
4Fe + 3O2 = 2Fe2O3
2. Kirjutame antud andmed reaktsioonivõrrandi kohale:
35 g V=?
4Fe + 3O2 = 2Fe2O3
3. Leiame raua ja hapniku molaarmassid:
4. Leiame raua moolid, kuna me teame raua massi:
5. Reaktsioonivõrrandi kordajate järgi leiame hapniku moolid:
6. Leiame hapniku ruumala:
Vastus: 35 grammi raua roostetamiseks kulub 21 dm3 hapnikku.
Lisainfo
Märkasid viga? Anna sellest teada ja teeme TaskuTarga koos paremaks!