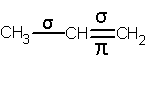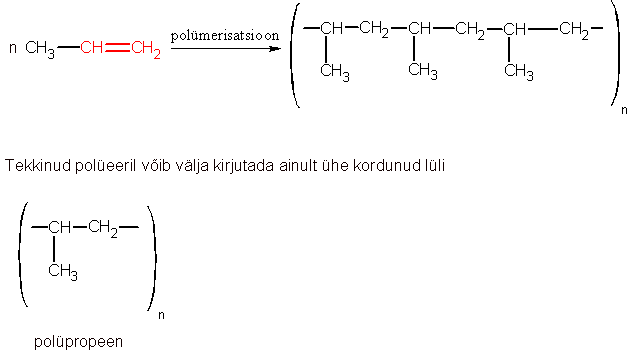Alkeenid ja alküünid. Küllastumata süsivesinikud
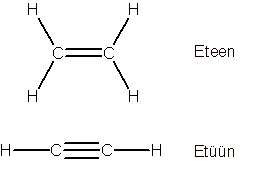
Küllastumata süsivesinikud on süsiniku ja vesiniku ühendid, kus süsinike vahel esineb kaksik- või kolmikside. Kaksiksidemega süsivesinikke nimetatakse alkeenideks ning kolmiksidemega süsivesinikke alküünideks. Kõige lihtsam alkeen on eteen ning kõige lihtsam alküün on etüün.
Kordne side koosneb kahest erinevast kovalentsest sidemest. Üks side on sigma-side (σ-side), mis on tugev side. Sama side esineb ka ühekordsel sidemel. Teiseks (ja kolmandaks alküünide puhul) on π-side, mis on tunduvalt nõrgem. Just π-side on see, mis määrab küllastunud ühendite keemilised omadused.
Sulle võivad huvi pakkuda need õppematerjalid:
Lahused
Ионы
Ioonid
Растворы
Oksüdatsiooniaste
Aatomid ja molekulid
Атомы и молекулы
Знакомство с химией
Tutvus keemiaga
Alkeenide ja alküünide nimetamine
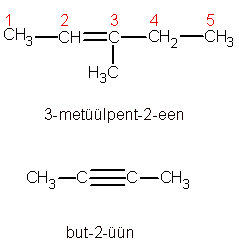
Nimetamise üldpõhimõtted on samad, mis alkaanidel. Alkeenide korral on tüviühendi nimetuse lõpp –een ning alküünide korral –üün. Kordse sideme asukoht näidatakse ära nii, et lisatakse selle süsiniku number enne järelliidet, peale mida kordne side asub. Näiteks:
Alkeenide ja alküünide füüsikalised omadused
Alkeenide ja alküünide omadused muutuvad homoloogilises reas sarnaselt alkaanide omadustele – molekulmassi suurendes suurenevad nii keemis- kui sulamistemperatuur ning tihedus. Toatemperatuuril on gaasilises olekus kolm esimest liiget, peale seda on tegemist juba vedelate ainetega. Alates sellest, kui süsinike aatomeid on 18, on tegemist tahkete ainetega. Nii nagu alkaanidki, küllastumata ühendid vees ei lahustu, kuna nad on hüdrofoobsed ained.
Alkeenide ja alküünide keemilised omadused
Kuna alkeenid ja alküünid sisaldavad kordset sidet, siis on nad keemiliselt palju aktiivsemad kui alkaanid. Peamine reaktsioon, mida küllastumata ühendid annavad on liitumisreaktsioonid vesinikuga (hüdrogeenimine), halogeenidega (halogeenimine), vesinikhalogeniididega ja veega (hüdraatumine). Kõik need reaktsioonid toimuvad ainult kuumutamisel katalüsaatori juuresolekul.
Näiteks propeeni hüdrogeenimisreaktsioon:
Eteeni hüdraatumisreaktsioon:
Lisaks eelpool nimetatud liitumisreaktsioonidele, võivad alkeenid anda ka liitumispolümerisatsiooni – reaktsioone, mille käigus ühinevad paljud ühe ja sama alkeeni molekulid ning tekib pika ahelaga ühend, kus üks ja sama ahelalõik pidevalt kordub. Selliseid korduvate ahelalõikudega (elementaarlülidega) pikki ühendeid nimetatakse polümeerideks ning ühendid, millest polümeer tekib on monomeerid. Alkeeni polümerisatsiooni korral alati katkeb kaksikside (tekib üksikside) ning tekkiva elementaarlüli põhiahelasse jäävad need kaks süsinikku, mille vahel kaksikside asus. Näiteks propeenist tekkiva polümeeri valem on järgmine:
Alkeenide ja alküünide tähtsamad esindajad
Eteen (CH2=CH2) on värvusetu nõrgalt uimastava toimega gaas. Peamiselt kasutatakse eteeni teiste ainete sünteesiks, kuid samas leiab kasutust ka toiduainetööstuses. Eteeni ja lämmastiku segu kiirendab puuviljade valmimist – meile saabuvad puuviljad enamasti pooltoorena ning nende valmimine toimub alles kohapeal eteeni ja lämmastiku segus.
Propeen (CH3CH=CH2) on värvusetu gaas, mis leiab peamist kasutust polümeeride valmistamisel. Polüpropeen on üks kõige levinum plastik, näiteks on sellest valmistatud kilekotid.
Isopreen ehk 2-metüülbuta-1,3-dieen on loodusliku kautšuki lähteaine, mida leidub palju kautšukipuus.
Etüün ehk atsetüleen (HC≡CH) on kõige enim kasutatav alküün. Etüün põleb hapnikus väga kõrge tempeatuuriga (3000 oC), mistõttu kasutatakse teda metallide lõikamisel ja keevitamisel.
VIDEOD:
Liitumispolümerisatsioon (ing)
Lisainfo
Märkasid viga? Anna sellest teada ja teeme TaskuTarga koos paremaks!